肺がん
肺がんについて
いわゆる「肺がん」とは、原発性肺癌を指します。肺を構成する組織のうちの、気管支や肺実質の上皮(内腔表面を覆う組織)から発生した「上皮性悪性腫瘍」です。
ここ最近の日本においては、原発性肺癌は1年あたり14万近く発症しており(がんの発生数としては3番目に多い)、1年あたり8万人弱の死亡者をだしています。日本人の死因のトップである「がん」のうち、最大の原因となっている疾患です。
数々の疫学調査から喫煙は最大の原発性肺癌の発生要因とされています。予防という観点からは、「喫煙しないこと」が日本全体での原発性肺癌の発生数を減少させ、特定の個人については原発性肺癌の発生確率を減少させる、各個人で達成し得る最大の手段となります。また、治療についても喫煙したままの状態では手術、抗がん薬治療、放射線治療のいずれの場合でも副作用や合併症を増やす原因にもなります。
肺がんの診療の流れ
原発性肺癌は、無症状の状態で検診や人間ドック、あるいは他の疾患の診療中に偶然に発見される場合があります。一方、慢性的な咳、血痰、呼吸困難感などの呼吸器症状、倦怠感や胸痛、意識状態の変調などの全身的な症状を契機に発見される場合もあります。
上記の肺癌を疑う異常を発見された場合、専門医療機関に紹介されることになります。当院では呼吸器内科が担当しております。受診の後、まず行われるのが「診断」です。診断の内容としては、大きくは以下の4つになります。
・「存在診断」=どこにどんな病変があるかの精査をします。
・「病理学的な確定診断」=その病変が原発性肺癌であるかどうか、また、原発性肺癌だとして、どのようなタイプなのかを精査します。
・ 「臨床病期診断」=原発性肺癌だとして、原発巣の大きさ、広がり、リンパ節転移の有無、他の臓器への遠隔転移の有無とその部位を調べます。
・「全身状態の把握」=「どれぐらい元気であるか」により治療の仕方も変わります。
これら4つの診断のための病歴聴取、身体所見、各種検査を順次行っていきます。その結果により、どのような治療が適切かを判断します。
肺がんの診断に必要な検査
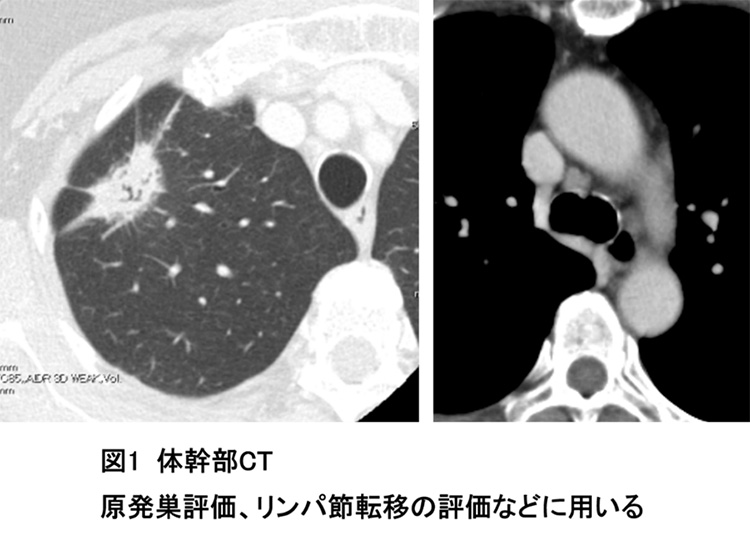
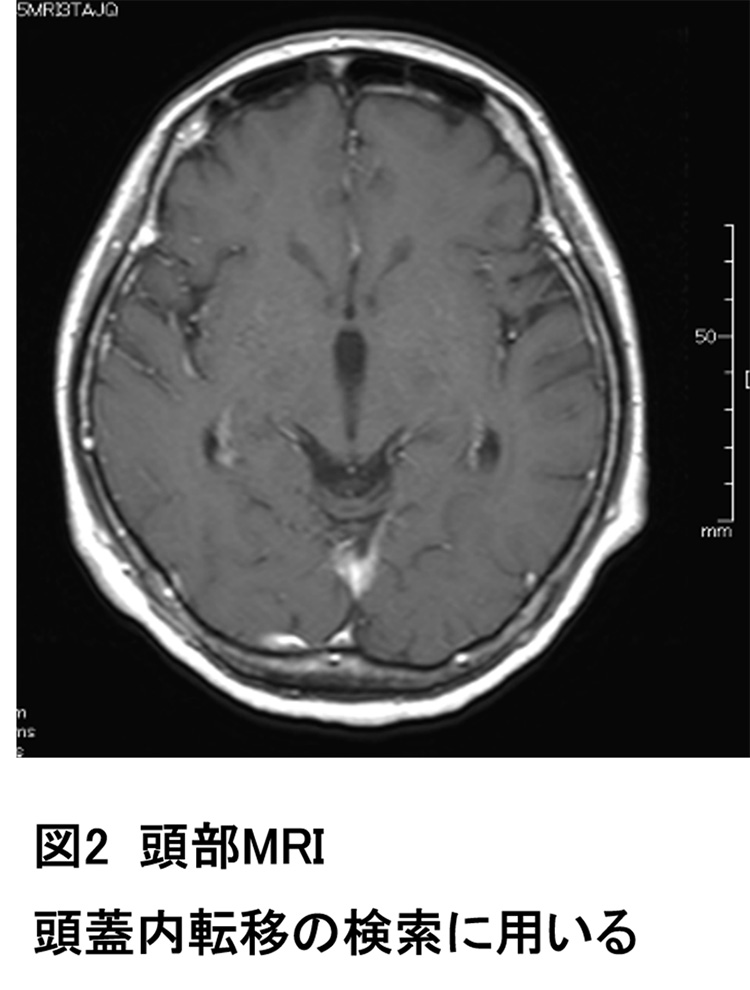
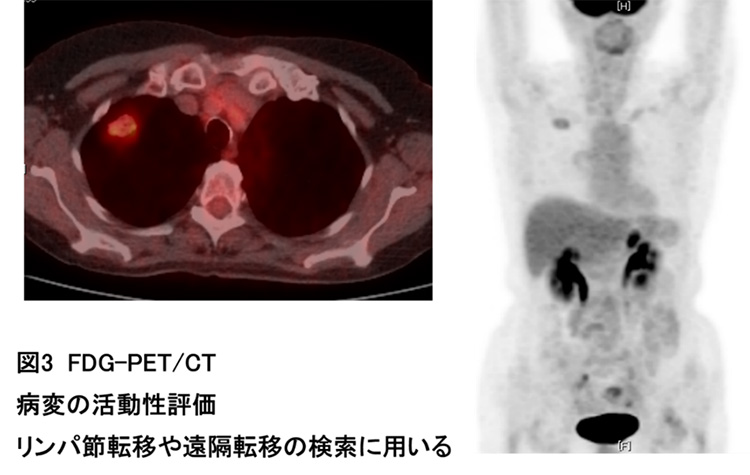
上記の診断のうち「存在診断」「臨床病期診断」に必要な検査として、体幹部(頸部~胸部~腹部)のCT検査 (図1)、頭部のMRI検査ないしはCT検査(図2)、FDG-PET/CT検査(院外)(図3)の3つの画像検査がほぼ必須となります。また、過去の検診などでレントゲンやCTの画像がある場合は、現在と過去の画像を比較し病変の経過を確認することは極めて重要です。
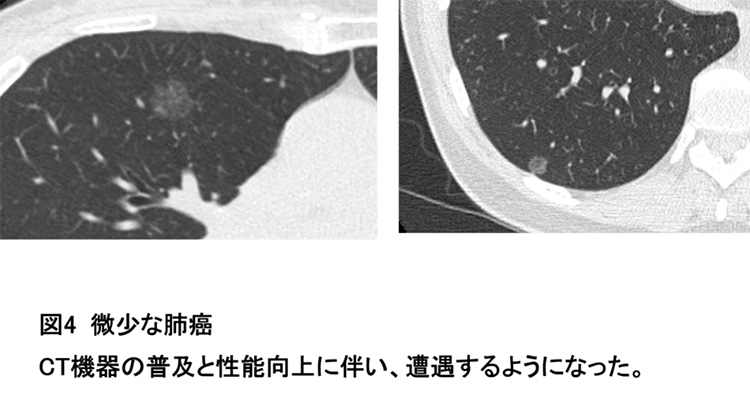
「病理学的な確定診断」には、「生検」(原発性肺癌を疑う病巣の一部を採取し、顕微鏡下に病変の良性/悪性、組織型を病理学的に診断する)が必要になります。生検する場所にあわせて、喀痰検査、気管支鏡、CTや超音波ガイド下肺生検、胸水穿刺などの方法を選択します。後述する遺伝子変異(耐性を含む)の問題もあり、なるべく組織診断をつけるようにしています。気管支鏡専用のCアーム透視台を備えた気管支鏡室にて気管支鏡検査(原則2泊3日)を行い、症例に応じて超音波気管支鏡(Endobronchial Ultrasonography:EBUS)や細経気管支鏡も活用し、診断確定率を上げるように努めています。胸壁に近い部位や気管支鏡では到達が難しい部位に関しては、放射線診断科に依頼してCTまたは超音波ガイド下生検や呼吸器外科に依頼して外科的生検などを行う場合もあります。また、CT検診などの普及により、生検が困難な小さい肺癌疑い病変が見つかることがあります(図4)。この場合は、「経過や画像所見で肺癌が強く疑われる」「肺癌だとした場合、切除が適応となる臨床病期」であれば、「生検」をスキップして確定診断を兼ねた切除術を行うこともあります。
近年は、生検で単に肺癌の診断をつけるのみだけでなく、遺伝子の変化、タンパク質の発現の有無や程度を調べることも行われています。現在、EGFR遺伝子変異、BRAF遺伝子変異、ROS1融合遺伝子、ALK融合遺伝子/タンパク質発現、PD-L1タンパク質発現が、肺がん薬物治療の選択肢決定の上で非常に重要な情報となっています。
「全身状態の把握」は、治療を進めるうえで非常に重要です。ECOG Performance status、既往歴(=過去に罹患した疾患)、併存症(今現在指摘されている、あるいは治療中の疾患)、喫煙歴、使用している薬剤、採血データ、呼吸機能検査、心電図などを確認し、治療の妨げになるような状態、あるいは治療において配慮すべき状態の把握をします。
治療方針
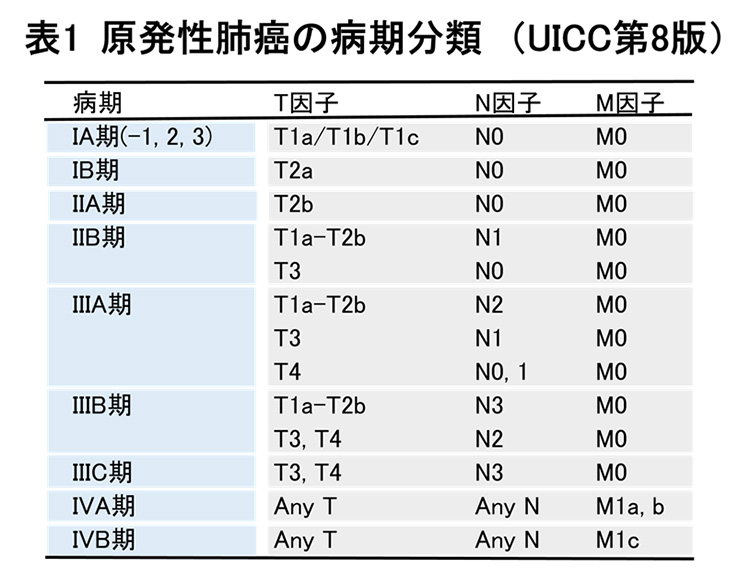
原発性肺癌の診断に必要な検査により、「原発性肺癌」あるいは「原発性肺癌が強く疑われる病変」の、タイプと進行度が判明します。それにより「臨床病期」と呼ばれる、治療開始前の原発性肺癌の進行度=「どこまで広がっているか」が判明します。臨床病期は国際的に統一された基準(表1)により病変の進行度を示すものです。その進行度により、基本的な治療方針が決定されます。患者さんの年齢や合併症、全身状態(Performance status:PS)などを考慮して、最新の肺がん診療ガイドラインに基づき、呼吸器内科、呼吸器外科や放射線治療科と相談した上、で治療方針を決定し、手術療法(外科的切除)、放射線療法、全身化学療法(抗がん剤)の選択または3者を組み合わせた集学的治療を行っています。
治療方針でまず重要になるのが、原発性肺癌のタイプです。原発性肺癌のうち、「小細胞癌」と呼ばれるタイプは、非常に進行が速いですが、放射線治療や抗がん薬が比較的効きやすいです。多くの場合は手術の適応にならず、放射線治療や抗がん薬による治療が中心です。しかし、切除による根治が期待できる病期(臨床病期I期)については手術と術後の抗がん薬投与の治療が選択されることもあります。
原発性肺癌のうち、「小細胞癌」と呼ばれるタイプ以外のものには、「腺癌」「扁平上皮癌」「腺扁平上皮癌」「大細胞内分泌癌」「肉腫様癌」などがあり、「非小細胞肺癌」と総称されます。腺癌、扁平上皮癌の二者で非小細胞肺癌の9割以上を占めます。非小細胞肺癌ですと、臨床病期I期、II期、III期の一部については手術治療が適応になります(表2)。手術適応にならないIII期は放射線治療と抗がん薬が治療の中心となり、IV期については抗がん薬が治療の中心となります。手術治療が適応となる場合でも術前あるいは術後に放射線治療や抗がん薬を必要とすることがあります。

手術治療
手術の適応とされる臨床病期I期、II期、一部のIII期の非小細胞肺癌に対しての手術治療は、治癒をもたらす可能性の最も高い治療法です。
切除の範囲ですが、肺癌の手術の基本は、肺癌病巣を含む肺葉(肺の袋)の切除=肺葉切除、および所属するリンパ節の郭清(決められた領域のリンパ節の切除)になります。しかし、病変の広がりのため、肺葉切除よりもさらに広い範囲の切除(二葉切除、一側肺全摘、隣接臓器の合併切除など)を必要とする場合もあります。
一方で、併存疾患や低肺機能のために、手術そのものは可能だが、標準的な手術である「肺葉切除」ができない場合があります。その場合は、「縮小手術」という、切除範囲を限定した切除方法がとられる場合があります。具体的には区域切除や楔状肺部分切除を行うことになります。これらの術式は肺の切除量を減らし、切除後の負担を減らすことができる反面、局所の再発の危険性が高くなることが知られています。さらに、臨床病期としては手術適応だが、手術そのものが困難という場合があります。その場合は、放射線治療などの非手術治療法が選択されます。
近年の画像診断の発達で、非常に小さい肺癌病変(図4)が発見される機会が増えており、「標準的な手術である肺葉切除より少ない範囲の切除である縮小手術でも、根治的な手術になり得る」場合があります。施設により適応される範囲が異なりますが、当院では、1) 腫瘍径が20 mm以下、2) 肺の末梢側に存在、3) FDG-PET検査での病変の活動性が低い、4) 術中のリンパ節の診断で転移がないこと、という条件が揃えば、適応としています。
切除するためのアプローチですが、ここ20年で、内視鏡手術(胸腔鏡と呼ばれるカメラを使用した手術、一般にVATS: videothoracoscopy-assisted thoracic surgeryと呼ばれる)で、小さい手術創にて行うことが一般的となっており、また、2018年4月より手術用のロボットを使用した、ロボット支援胸腔鏡下の手術(RATS: robot-assisted thoracic surgery)も保険適応となっております。当院呼吸器外科でも、VATSによる手術を基本とし、症例によりダビンチXiという手術用ロボットを使用したRATSによる手術を行っております。
一方で、肺門部(肺の付け根)に浸潤する肺癌や非常にサイズの大きい肺癌、気管支や血管の再建が必要な場合は、開胸手術、場合によって肋骨を切断して肋間を開けて行う手術が必要になります。患者さんそれぞれによって適切なアプローチ方法を選択して行うことになります。
手術適応になる臨床病期の場合でも、病変の進行度や部位により、手術の前、あるいは後に内科的な治療を要する場合があります。
1) 肺尖部胸壁浸潤肺癌:
肺尖部と呼ばれる胸腔の頂上の部分に浸潤する肺癌で、手術の前に放射線+化学療法を行った後に、切除術を行うことが推奨されています。
2) 縦隔リンパ節転移のある肺癌:
臨床病期で、N2-IIIA期の肺癌です。手術の前に化学療法、あるいは放射線+化学療法を行った後に切除を行うことを考慮してもよいとされています。比較的体力のある若い患者さんで考慮されます。
3) 術後補助化学療法:
切除の結果、病理学的にIB期、あるいはサイズのみのIIA期、IIB期については、内服抗がん薬であるUFTを2年間内服することが推奨されています。当院でも、患者さんの状態や内臓機能に問題がなければ内服治療を受けていただいています。また、病理学的にIIB期(胸壁浸潤や肺内転移あり)、III期であった場合、シスプラチンを含む点滴抗がん薬による治療が推奨されます。当院では、患者さんの内臓機能が十分耐えられるであろうと判断した場合、シスプラチン+ビノレルビンによる術後補助化学療法を行っています。
さらに近年の試験で、腫瘍組織の検索でPD-L1というタンパク質が高発現している場合は、免疫チェックポイント阻害薬の一つであるアテゾリズマブの投与で再発率の低下が示されました。また、腫瘍細胞にEGFR遺伝子変異がある場合は、EGFR特異的チロシンキナーゼ阻害薬であるオシメルチニブの内服投与で再発率の低下、生存率の向上が示されました。当院でも上記条件が適応する患者さんに実施しております。
4) サルベージ手術:
臨床病期で手術の適応にならない場合であっても、内科的治療に伴い、手術が可能になるほど腫瘍が縮小する場合があります。また、内科的治療が非常に有効だったが局所のみの再増大で切除が可能、という場合もあります。そのような場合に手術を行うものをサルベージ手術と呼んでいます。技術的な難易度が高く、また、患者さんの状態が良好であることが必須ですが、「根治」を目指せる治療として、近年施行例が増えています。当院呼吸器外科でも、呼吸器内科、放射線治療科と協力し、適応となる例にはサルベージ手術を行っております。
化学療法・放射線療法
① 化学療法(非小細胞肺癌)
手術適応がないと判断された臨床病期ⅢA~ⅢCの非小細胞肺癌においては、化学療法(カルボプラチン+パクリタキセル、シスプラチン+S-1など)と放射線療法の併用(同時化学放射線療法)が推奨されます。臨床病期ⅢA~ⅢCは「根治」を目指せる病期であり、同時化学放射線療法後に病勢進行がない患者さんに対しては、免疫チェックポイント阻害薬の1つであるデュルバルマブによる1年間の維持療法を行うことが2018年より標準治療となりました。
一方、臨床病期Ⅳ期の非小細胞肺癌の標準治療は薬物療法になりますが、近年多くの新薬が承認され使用可能となっています。以前はEGFR、ALKの遺伝子変異に対してのみ分子標的薬が使用可能でしたが、最近になってROS1、BRAF、METに対する分子標的薬が登場し、さらにKRAS、HER2、RETなどに対する分子標的薬も今後承認される予定です。このように続々と登場する分子標的薬の適応となるかどうかを調べるために、当院では次世代シークエンサー(オンコマインDx Target Testシステム)を用いてEGFR、ALK、ROS1、BRAF、METを含めた46遺伝子変異を網羅的に検査し、治療に役立てています。EGFR、ALK、ROS1、BRAF、METの変異を検出した患者さんに対しては、各々対応した分子標的薬を使用した治療を行っています。また、これらの遺伝子変異がない患者さんに対しては、免疫チェックポイント阻害薬(ニボルマブ、ペムブロリズマブ、アテゾリズマブ)、殺細胞性抗癌剤が治療の軸となり、可能な患者さんでは免疫チェックポイント阻害薬と殺細胞性抗癌剤の併用療法を行います。
このように非小細胞肺癌の治療の進歩はとても進んでおり、当院でも各抗癌剤に伴う副作用に対しても適切な支持療法を行いながら、各患者さんに応じた最適な治療を行っています。
② 化学療法(小細胞肺癌)
病変の広がりに応じて、限局型小細胞肺癌と進展型小細胞肺癌に分けられます。限局型に対しては同時化学放射線療法を行って根治を目指します。進展型小細胞肺癌に対しては長年殺細胞性抗癌剤が標準治療となっていましたが、2018年に殺細胞性抗癌剤と免疫チェックポイント阻害薬(アテゾリズマブ、デュルバルマブ)の併用療法が承認され、標準治療となっています。
③ 放射線療法
上記の化学療法との併用のみならず、骨転移や脳転移に対する緩和的放射線照射(必要に応じてガンマナイフ(院外))も行っています。
院内がん登録統計
院内がん登録についての説明はこちら。

